Что такое таргетная терапия?
Таргетная терапия — это тип лечения рака, который направлен на конкретные биохимические процессы в раковых клетках, которые помогают им расти, делиться и распространяться.
Этот вид лечения предусматривает использование высокоспецифичных молекул, воздействующих на конкретный компонент биохимической реакции внутри клетки, который и представляет собой «цель» (англ.target).
Чаще всего таргетные препараты — это молекулы, блокирующие определенные (присущие исключительно конкретному виду опухоли) внутриклеточные ферменты — киназы.
Также многие (но не все) лекарства для таргетной терапии — это биосинтетические препараты. Поэтому методы таргетной терапии с использованием таких препаратов одинаково правильно будет назвать и биотерапевтическими, и иммунотерапевтическими.
Типы таргетной терапии, используемые в Европе
Наиболее целевой терапией являются либо низкомолекулярные препараты, либо моноклональные антитела.
- Низкомолекулярные лекарства достаточно малы, чтобы легко проникать в клетки, поэтому они используются для целей, которые находятся внутри клеток.
- Моноклональные антитела, также известные как терапевтические антитела, представляют собой белки, вырабатываемые в лаборатории. Эти белки предназначены для прикрепления к конкретным мишеням, обнаруженным на мембранах раковых клетках. Некоторые моноклональные антитела маркируют раковые клетки, так что они будут лучше видны и разрушены иммунной системой. Другие моноклональные антитела непосредственно препятствуют росту раковых клеток или вызывают их самоуничтожение.
При каких видах рака в Европе используют таргетную терапию
Таргетная терапия работает в том случае, если при конкретном виде онкозаболевания выделена целевая мишень и создан препарат, воздействующий на эту мишень.
Так, например, таргетная терапия колоректального рака направлена на блокирование фактора роста эндотелия сосудов (VEGF) и рецептора эпидермального фактора роста (EGFR). На ту же мишень направлена и таргетная терапия рака молочной железы. Однако рецепторы EGFR в первом и во втором случае имеют разное строение и потому препараты для них используются тоже разные.
А вот таргетная терапия меланомы чаще всего основана на блокировании ферментов тирозинкиназ, а также внутриклеточных путей передачи сигналов от мембраны к ядру. При раке почек таргетная терапия предусматривает использование ингибиторов фолатных α-рецепторов.
Причем в каждом случае речь не идет о любой меланоме или любом раке почек, а только о конкретных его генетических подвидах. Для каждого генетического типа рака требуется свой препарат.
Для многих видов онкозаболеваний лекарства уже разработаны. Для других еще только разрабатываются.
Как таргетная терапия работает против рака
Большинство целевых методов лечения воздействуют на определенные белки-ферменты, которые помогают опухолям расти и распространяться по всему телу. Но существуют разные точки приложения таргетной терапии.
- Помощь иммунной системе в уничтожении раковых клеток. Одна из причин того, что раковые клетки процветают, заключается в том, что они способны скрываться от вашей иммунной системы. Определенные целевые методы лечения могут маркировать раковые клетки, поэтому иммунной системе легче находить и уничтожать их.
- Остановка роста раковых клеток. Здоровые клетки в вашем теле обычно делятся, чтобы создать новые клетки, только когда они получают центральные сигналы для этого. Но у некоторых раковых клеток есть изменения в белках на их мембране, которые подают команду на деление в отсутствии центральных сигналов. Таргетные препараты блокируют активность таких белков и не дают раковым клеткам делиться. Этот процесс помогает замедлить неконтролируемый рост рака.
- Остановка роста сосудов внутри опухоли. Опухоли должны образовывать новые кровеносные сосуды, чтобы их клетки могли получать питание и новообразование могло расти. Новое семейство лекарств для таргетной терапии — ингибиторы ангиогенеза — предназначено для вмешательства в эти сигналы, чтобы предотвратить формирование кровоснабжения опухоли.
- Причины смерти раковых клеток. Здоровые клетки гибнут, когда они повреждены или больше не нужны организму. Но у раковых клеток есть способы избежать этого процесса. Таргетная терапия может заставить раковые клетки вновь включать подавленный механизм самоуничтожения.
Основные проблемы таргетной терапии
- Развитие устойчивости к препарату. По этой причине целевая терапия может работать лучше всего при использовании с другими целевыми терапиями или с другими видами лечения рака, такими как химиотерапия и облучение.
- Препараты для некоторых целей трудно разрабатывать. Причины включают структуру цели, функцию цели в клетке или оба фактора.
Побочные эффекты и последствия таргетной терапии в онкологии
Побочные эффекты при этом виде лечения могут зависеть от типа целевой терапии и от того, как организм реагирует на эту терапию.
Наиболее распространенные побочные эффекты целевой терапии — диарея и проблемы с печенью. Другие побочные эффекты могут включать проблемы со свертыванием крови и заживлением ран, высокое кровяное давление, усталость, язвы во рту, изменения ногтей, потерю цвета волос и проблемы с кожей. Проблемы с кожей могут включать сыпь или сухость кожи.
Большинство побочных эффектов таргетной терапии бесследно проходят после окончания лечения.
Кроме того, существует множество лекарств, способных существенно снизить выраженность побочных эффектов таргетной терапии.
Преимущества таргетной терапии в Бельгии
- Доступ к широкому спектру новейших таргетных препаратов сразу же после одобрения Европейским медицинским агентством (EMA). Это очень важно в том случае, если у пациента диагностирована метастазирующая или неоперабельная опухоль, против которой до появления нового препарата не было таргетного лекарственного агента.
Или тогда, когда один курс препаратом прошлого поколения уже пройден, и препарат срочно необходимо сменить из-за развития устойчивости к нему опухоли.
- Возможность комплексного лечения. Работы по комбинированию методов таргетной терапии ведутся сразу в нескольких онкологических центрах Бельгии.
Сочетание этого типа лечения с другими современными видами терапии рака обеспечивает повышение эффективности, а нередко и снижение токсичности.
- Возможность воспользоваться экспериментальными программами лечения.
В Бельгии проводится достаточно много исследований новых перспективных препаратов, которые могут помочь сохранить жизнь тогда, когда другие варианты уже исчерпаны. Кроме того, участие в таких программах дает возможность получить лечение бесплатно.
- Стоимость таргетной терапии.
Цена на лекарства для лечения рака таргетной терапией до сих пор остается высокой.
Клиники Бельгии, в которых используются современные методы таргетной терапии
Для получения подробной информации о возможности лечения таргетной терапией в Бельгии, а также о ценах на препараты и стоимости курса, отправьте нам сообщение через форму обратной связи или закажите обратный звонок. Вся информация предоставляется нами бесплатно.
Источник: https://BelHope.ru/napravleniyamediciny/onkologiya-diagnostika-i-lechenie-raka/targetnaya-terapiya
Что происходит с опухолью при таргетной терапии
Таргетная терапия при раке подразумевает сложный механизм воздействия на патологические клетки. В основе лежит влияние на ДНК патогенные структуры и другие элементы, поддерживающие жизнедеятельность и размножение опухоли.
Главное, чего смогли добиться разработчики таргетного способа лечения, — ограничить нормальные ткани от воздействия противораковой терапии. Обмен веществ, иммунитет, общее состояние не страдают от этих препаратов.
Медикаменты подбираются в зависимости от генных особенностей злокачественного новообразования, поскольку их подбирают, исследуя мутации генов и генные дефекты. Средства уничтожают центры раковых клеток, отвечающие за размножение и формирование органелл, а также рецепторы, с которыми связываются атипические ткани.
Преимущества таргетной терапии
Таргетная терапия отличается от химиотерапии рака за рубежом тем, что не оказывает воздействия на здоровые клетки. Например, принцип действия некоторых химиопрепаратов заключается в остановке размножения быстрорастущих клеток в организме.
А к таковым относятся и клетки волос, из-за чего происходит облысение, и клетки кожи, из-за чего кожа выглядит намного старше своего возраста. Таргетная терапия показана и в тех случаях, когда пациент очень слаб. Такой подход к назначению применяют в ведущих клиниках Израиля, Германии и Швейцарии.
Показания
Таргетное лечение используется в случаях метастазирования, которое не реагирует на химиотерапию и облучение.
Таргетное лечение назначается только при раке легких, почек, груди, кожи и при меланоме. Для других локализаций лекарство неэффективно, что ограничивает круг его назначения. Их применяют при таких состояниях:
- в случаях неоперабельной опухоли;
- выраженная агрессивность новообразования;
- истощение организма пациента от химиотерапии и облучения;
- рецидив рака после успешного лечения;
- множественные метастазы, нечувствительные к химиопрепаратам и лучевой терапии.
Принцип действия таргетной терапии
- Принципиальное отличие таргетных от классических противоопухолевых препаратов цитотоксического действия (алкилирующие агенты, антиметаболиты,
- , винкаалкалоиды, таксаны, ингибиторы топоизомеразы) состоит в том, что первые действуют направленно на молекулы, участвующие в процессе канцерогененза, а вторые, также обладающие специфической направленностью, имеют своей точкой приложения такие общебиологические процессы, как синтез
- и митоз.
- иматиниба мезилат (Гливек), гефитиниб (Иресса), эрлотиниб (Тарцева), сунитиниб (Сутент), лапатиниб (Тайкерб), дазатиниб (Спрайсел), сорафениб (Нексавар), нилотиниб (Тасигна), темсиролимус (Торисел), эверолимус (Афинитор);
- короткие синтетические отрезки ДНК, связывающиеся с рибонуклеиновой кислотой (РНК), — антисмысловые нуклеотиды: облимерсен (Генасенс); природные соединения (Неовастат, флавоперидол); вирусы (AdP53, ONIX-015).
- 1) нацеленные на пути передачи сигнала в опухолевой клетке2) нацеленные на уникальный фенотип опухолевой клетки.
Последняя группа включает используемые в онкогематологии МКА, распознающие и блокирующие специфические нерецепторные антигены на поверхности клеток и оказывающие прямое цитотоксическое действие на эти клетки.
К таким препаратам относятся гуманизированное мышиное антитело к поверхностному антигену CD20 В-клеток — ритуксимаб (Мабтера), с успехом используемое при В-клеточных неходжкинских лимфомах (НХЛ) и хроническом лимфолейкозе (ХЛЛ), а также гуманизированное мышиное МКА алемтузумаб против гликопротеида CD52 на поверхности В- и Т-клеток, естественных киллеров (NK), моноцитов и макрофагов, также используемое при В-клеточном ХЛЛ.
Предлагаем ознакомиться: Болезни глаз у кур: симптомы и их лечение, фото
На базе этих МКА созданы конъюгаты с токсинами — гемтузумаб озогамицин (Милотарг), а также радиоиммуноконъюгаты — ибритумомаб тиуксетан (Зевалин) и 13,1 тозитумомаб (Бексар).
Основной принцип действия таргетных препаратов первой группы, т.е. блокирующих передачу сигнала, базируется на том, что в норме лиганды (молекулы гормонов, цитокинов, факторов роста и др.
) взаимодействуют с рецепторами клетки, а те передают сигнал через сеть молекул, преимущественно белковых киназ к ядру, что определяет способность клетки к пролиферации, дифференцировке, апоптозу, адгезии, ангиогенезу.
HER1, ErbB1), EGFR2 (HER2, ErbB2), EGFR3 (HER3, ЕгЬВЗ), EGFR4 (HER4, ErbB4). Рецепторы представляют собой гликопротеиды, состоящие из трех доменов: экстрацеллюлярного, обладающего способностью связываться с лигандом, трансмембранного и интрацеллюлярного, обладающего тирозинкиназной активностью.
При связывании лиганда, например EGF, с экстрацеллюлярным доменом рецептора происходит димеризация, т.е. объединение двух связанных с лигандом рецепторов в единый функциональный комплекс с последующим аутофосфорилированием тирозинкиназы внутриклеточного домена рецептора, что обеспечивает передачу сигнала внутрь клетки и затем внутриклеточную передачу его к ядру.
- • блокаду циркулирующих лигандов;• блокаду связывания лигандов с экстрацеллюлярным доменом рецептора;• ингибицию тирозинкиназ внутриклеточного домена рецептора, что ведет к блокаде фосфорилирования, нарушая передачу сигнала от рецептора к молекулам, осуществляющим внутриклеточную передачу сигнала;• внутриклеточную ингибицию белков, осуществляющих интрацеллюлярную передачу сигнала.
- Примером блокады путем нейтрализации лиганда до его возможного связывания с рецептором служит применение бевацизумаба — МКА к фактору роста эндотелия сосудов (VEGF), циркулирующему в крови; примером блокады путем конкурентного связывания с экстрацеллюлярным доменом рецептора — использование МКА к EGFR1 цетуксимаба и панитумумаба.
- Трастузумаб — МКА к рецептору HER2, лиганд которого неизвестен, блокирует этот рецептор, связываясь с его экстрацеллюлярным доменом.
- Блокаду активности внутриклеточного домена EGFR1 осуществляют малые молекулы — ингибиторы тирозинкиназэрлотиниб и гефитиниб.
Двойной ингибитор тирозинкиназ лапатиниб блокирует активность внутриклеточного домена рецепторов EGFR1 и HER2 (EGFR2).
Внутриклеточную блокаду передачи сигнала осуществляют мультитаргетные ингибиторы киназ иматиниб, дазатиниб, сунитиниб, сорафениб, причем два последних препарата ингибируют рецепторы VEGF и тромбоцитарного фактора роста (PDGF), оказывая антиангиогенное действие, благодаря чему их обычно относят к антиангиогенным препаратам.
Ингибиторы белка mTOR (мишень рапамицина у млекопитающих), внутриклеточной серин-треониновой киназы, регулирующей пролиферацию клеток и ангиогенез, темсиролимус и эверолимус оказывают противоопухолевое действие при раке почки.
В процессе развития опухоли важнейшую роль играет неоангиогенез, определяющий возможность роста и метастазирование опухоли и, соответственно, служащий перспективной мишенью таргетной терапии. Наиболее практически ценным препаратом из группы ингибиторов ангиогенеза оказался бевацизумаб — рекомбинантное гуманизированное МКА к VEGF.
Блокада VEGF с помощью бевацизумаба ведет к ингибиции неоангиогенеза и вызывает противоопухолевый эффект при колоректальном раке (КРР), раке молочной железы (РМЖ), раке почки, немелкоклеточном раке легкого (НМРЛ).
Ктаргетным относятся также препараты, влияющие на деградацию белков, в частности действующие на протеасомы. При миеломной болезни с успехом используется бортезомиб (Велкейд), ингибирующий функцию протеасомы 26S, которая отвечает за внутриклеточную деградацию белка.
Таргетная химиотерапия имеет несколько направлений в своем действии.
- Первое – блокировка деления раковой клетки. Лекарства разрушают сложившиеся процессы на биохимическом уровне, берут под контроль жизнедеятельность раковой клетки, не дают ей разможаться и расти.
- Второе – остановка процесса деления раковых клеток и, как следствие, невозможность поражать новые области организма. Для роста, деления, питания раковых клеток нужны собственные кровеносные сосуды. Новая таргетная химиотерапия препятствует их образованию.
- Третье – регулировака иммунных процессов в организме человека. Терапия помогает иммунитету распознавать клетки рака, которые были образованы из здоровых клеток организма и не были распознаны как проблема. В этом случае можно рассматривать таргетную терапию как прививку. В организм вводят микродозы мертвых клеток рака и организм сам учится отличать здоровые клетки от мутировавших.
Методы и проведение
Сорафениб применяется при заболевании молочной железы, препятствуя питанию опухоли через гормональные рецепторы.
Таргетная терапия имеет свои особенности при разной локализации рака:
- Опухоль молочной железы требует применения таких препаратов: «Тамоксифен», «Торемифен», «Фулвестрантом», «Сорафениб». Эти лекарства имеют различные механизмы воздействия, но одну цель — снизить поступление эстрогена и прогестерона в опухоль, чтобы они не связались с гормональными рецепторами, поскольку опухоль зависит от женских половых гормонов.
- Рак почек включает такие таргетные медикаменты: «Авастин», «Нексавар», «Торисел». Терапия направлена на предупреждение формирования сосудистой сети в опухоли, чтобы не возникло распространения метастазов по кровеносной системе. Если заблокировать капилляры в образовании, клетки не смогут делиться, размножаться и со временем погибают.
- При карциноме легких назначают «Авастин», «Сорафениб», «Эрлотиниб» с целью остановки роста новообразования, профилактики метастазирования и инвазии рака. Диагностика опухоли легкого часто происходит, когда операция невозможна. Тогда таргетная терапия улучшает состояние пациента и предотвращает распространение опухолевых клеток.
Предлагаем ознакомиться: Если дышать разложившейся опухолью животного
Побочные эффекты таргетной терапии
Таргетная терапия намного менее токсична, чем классическая химиотерапия. Но есть некоторые побочные эффекты, которые могут проявляться при использовании ее:
- диарея,
- заболевания печени, вплоть до гепатита,
- изменение в структуре волос и ногтей,
- сухость кожи,
- угревая сыпь,
- высокое кровяное давление,
- проблемы со свертываемостью крови,
- усталость,
- тошнота,
- боли в суставах,
- репродуктивные проблемы у женщин.
Будущее таргетной терапии
Во всем мире таргетная терапия считается очень прогрессивным методом лечения рака. Уже сейчас методика применяется при лечении рака в Израиле и других странах с развитой системой здравоохранения. Есть надежды на полное излечение рака не только на ранних стадиях, но и на третьей и четвертой стадии, которые известны свей тяжестью из-за начала метастатического процесса.
- Рак почек
- Рак печени
- Меланома
- Опухоли кишечника.
Так же есть прогресс в лечении рака рака щитовидной железы за рубежом, который практически не лечится медикаментозно.
В настоящее время ведется большое количесство исследований в области молекулярно-генетической терапии рака. Что дает надежду на полное избавления человечества от такого грозного врага как рак.
Ограничения
Терапия является эффективной не для всех видов рака, например, при злокачественном образовании толстой кишки не используется.
Таргетную терапию не применяют в таких случаях:
- новообразование другой локализации — не легкие, печень, грудь или кожа;
- индивидуальная непереносимость препаратов;
- иммуногистохимические результаты, указывающие на резистентность раковых клеток к таргетным медикаментам.
Плюсы и минусы
Положительные стороны таргетного лечения:
- Отсутствие влияния лекарственных средств на нормальные клетки организма пациента.
- Возможность отменить химиотерапию.
- Вариант прохождения терапии дома, поскольку медикаменты выпускаются в таблетированной форме.
- Высокая результативность на ранних этапах лечения.
- Возможность комбинирования с другими способами терапии.
- Каждый препарат влияет на отдельное звено опухолевого процесса, поэтому можно корректировать лечение.
- Улучшение состояния больного в случае неоперабельного рака или невозможности применения химиотерапии или облучения.
К минусам относится высокая стоимость лекарственных средств и необходимость проведения ряда диагностических мероприятий для правильного подбора медикаментов, что также составляет значительную цену. Этот метод лечения применяется только при раке легких, почек, молочной железы, кожи, меланоме, что сужает круг назначения.
Источник: https://neonkologia.ru/proiskhodit-opukholyu-targetnoy-terapii/
Таргетная терапия в онкологии
Таргетная терапия – одна из новейших разработок в области лечения рака, является одним из значительных направлений медикаментозного лечения онкологии.
Она заключается в воздействии исключительно на клетки опухоли, что мешает дальнейшему росту и распространению злокачественного поражения. Данный метод лечения может использоваться как самостоятельно, так и в сочетании с химиотерапией.
Это зависит от каждого конкретного случая, а именно от вида и локализации опухоли.
Что такое таргетная терапия в онкологии
Данная технология лечения рака относительно новая, ей не более 50 лет. В перевод с английского название можно истолковать как «удар по конкретной цели», то есть действие на пораженные клетки, минуя здоровые.
Этот вид терапии воздействует исключительно на пораженные клетки, минуя здоровые, вернее действие таргетной терапии в онокологии направлено непосредственно на специфические молекулы в организме, из-за которых растут и размножаются раковые клетки.
Кроме того, таргетные препараты перекрывают доступ кислорода к опухолевым тканям, что так же мешает дальнейшей жизнеспособности пораженных клеток.
Благодаря этому способу лечения перестает расти не только сама опухоль, но пресекается и распространение метастазов.
На сегодняшний день существуют вариации лечения раковых опухолей при помощи таргетной терапии:
- Нарушение работы структур, поддерживающих опухолевые клетки жизнеспособными;
- Действие только на пораженные клетки, включая рецепторы, гены и различные внутриклеточные ферменты;
- Уничтожение сигнального пути для раковых клеток, что мешает их жизни и размножению.
Таргетная терапия воздействует исключительно на пораженные клетки
Данный способ лечения может применяться как самостоятельно, так и в комплексе с химиотерапией для увеличения шансов на благоприятный прогноз. Таргетная терапия менее токсична, чем химическая или лучевая, но все же имеет свои побочные эффекты.
Показания к назначению
Решение о том, можно ли в каждом конкретном случае заболевания использовать таргетные препараты принимает специалист. Это зависит от строения клеток опухоли, ее локализации, общего состояния пациента и ряда других факторов.
В основном лечение таргетными веществами назначается в следующих случаях:
- Когда в лечении нуждается пациент пожилого возраста или находящийся в тяжелом состоянии. То есть, в таких ситуациях, когда лечение при помощи химиотерапии противопоказано;
- При необходимости стабилизировать процесс развития злокачественной опухоли и трансформировать его из активного в хронический;
- Для профилактики рецидивов рака, а так же, чтобы остановить распространение метастазов;
- Параллельно с лучевой или химиотерапией, чтобы снизить нагрузку от этих, более токсичных для организма, методов лечения.
Для того, чтобы выяснить целесообразность использования таргетной терапии, проводится молекулярно-генетический анализ злокачественных клеток. Это необходимо, для того, чтобы выяснить, есть ли в клетках то, что может быть целью для применения терапии.
Чаще всего данный метод лечения назначается, если химиотерапия не помогла (то есть рост опухоли так и не остановился), при наличии большого количества метастазов или при 4 стадии развития ракового заболевания.
Механизм воздействия
Методы воздействия таргетной терапии на опухоли различной локализации несколько отличаются.
Так, например, при раке молочной железы вводятся таргетные гормоны, несущие программу уничтожения раковых клеток, либо ведется терапия, убивающая гормоны, необходимые для разрастания и распространения опухоли.
При немелкоклеточном раке легкого пациенту вводятся средства, воздействующие на белки, необходимые для размножения пораженных клеток. То же самое происходит и при меланоме. Сначала выявляются типы мутации белков, а затем вводятся вещества, которые будут уничтожать такие белки.
В итоге у опухоли не остается ресурсов для жизнедеятельности, и ее развитие приостанавливается, а у пациента наступает стадия ремиссии.
К числу «мишеней», которые могут поражать таргетные препараты, можно отнести следующие:
- Мутировавшие гены, благодаря которым злокачественные клетки могут расти и делиться;
- Молекулы, несущие информацию о запрограммированной гибели клеток;
- Рецепторы к различным гормонам, находящиеся на поверхности злокачественных клеток (при опухоли груди);
- Рецепторы, отвечающие за развитие системы сосудов, необходимой для жизнедеятельности опухоли.
По химическому составу таргетные препараты можно разделит на два вида: малые молекулы и антитела.
Малые молекулы создаются синтетическим путем в лабораторных условиях. Они могут попадать внутрь пораженной клетки и там по необходимости воздействовать на бели, ДНК или РНК. Эти средства стоят дешевле, чем препараты, относящиеся к классу антител. Одно из их наиболее частых применений – профилактика метастазов при раке центральной нервной системы.
Антитела
Антитела – это белки, которые получаются вследствие развития иммунитета у животных (в основном мышей) к отдельным видам злокачественных заболеваний. Для того, чтобы человечески организм не отторгал такой белок, с ним проводят различные генетические модификации. Для простоты усваивания препарата такой белок можно встроить в иммуноглобулин – естественное вещество для человеческого организма.
Препараты
Для проведения таргетной терапии используются различные препараты в зависимости от строения и локализации опухоли.
Герцептин
Использование данного препарата увеличивает выживаемости практически вполовину, а также снижает вероятность рецидивов. Наиболее эффективно применение препарата в комплексе с химиотерапией.
Иматиниб
Применяется при лечении злокачественных опухолей желудочно-кишечного тракта, а также для борьбы с хроническим миелолейкозом.
Иматиниб – один из препаратов таргетной терапии
Ритуксимаб
Данный препарат используется при лечении Неходжкинских лимфом.
Тайверба
Наиболее часто назначается при лечении метастатических и обширных опухолей молочной железы, особенно, если пациент до этого уже получал химиотерапевтическое лечение. Кроме того, препарат может использоваться для лечения опухолей мозга с метастазами.
Авастин
В основном используется в комплексе с химиотерапевтическим лечением, значительно повышая его эффективность. Особенно при опухолях легких, почек, молочной железы, толстой кишки и головного мозга.
Данное лекарство мешает разрастаться сосудам, которые необходимы для существования злокачественной опухоли. Таким образом, рак перестает расти, а со временем и вовсе переходит в стадию ремиссии.
Сорафениб
Применяется для борьбы с раком почек. Благодаря данному препарату опухоль перестает расти, а общее самочувствие пациента улучшается.
Тарцева
В основном применяется при злокачественных опухолях легких, если стандартная химиотерапия не подействовала. Препарат устраняет такие симптомы, как боль в груди, кашель и одышка. Кроме того, его применение значительно снижает темпы разрастания опухоли, благотворно отражается на самочувствии пациентов и увеличивает продолжительность жизни.
Тарцева
Данное лекарство также вполне успешно используется при лечении меланомы, рака почек с метастазами, опухолях печени, поджелудочной железы, пищевода и не только.
Иресса
В большинстве случаев способствует уменьшению опухоли. Чаще всего используется при лечении женщин, больных раком легких, которые до этого не курили. Нередко применяется в комплексе с другими препаратами для химиотерапии. Может применяться, в том числе для улучшения самочувствия пациентов, на которых не подействовала стандартная химиотерапия.
При каких видах рака используют
Таргетная терапия используется как в комплексе с химиотерапевтическим лечением, так и самостоятельно, против тех видов опухолей, в клетках которых обнаружен белок «мишень», на который смогут воздействовать таргетные вещества. К таким видам опухолей можно отнести следующие:
- Меланома;
- Колоректальный рак;
- Метастатический рак легкого;
- Плоскоклеточные разновидности злокачественных опухолей;
- Рак желудка и поджелудочной железы;
- Развитие злокачественной опухоли груди;
- Рак почек.
И это далеко не полный список, ведь данный метод терапии достаточно новый и специалисты до сих пор продолжают исследования, а также ведут наблюдения по поводу эффективности сочетаний таргетных препаратов между собой, а так же со стандартными химиотерапевтическими средствами.
Преимущества и недостатки терапии
У данного способа лечения есть свои преимущества и недостатки. К плюсам таргетных препаратов можно отнести следующие:
- Повышают эффективность при использовании совместно с химиотерапевтическим лечением;
- Практически не задевают своим воздействием здоровые клетки, что снижает количество негативных эффектов;
- Работают даже при запущенных формах рака, увеличивая срок жизни на месяцы, недели, а иногда и годы;
- Форма выпуска большинства средств – таблетки, что позволяет не травмировать дополнительно организм пациента;
- Действуют даже на те злокачественные клетки, которые нечувствительны или мало чувствительны к химическим препаратам.
Среди недостатков можно выделить следующие:
- Таргетные препараты нельзя использовать для широкого круга пациентов, в каждой ситуации лекарство необходимо подбирать индивидуально;
- Для того чтобы лечение оказалось эффективным, необходимо правильно подобрать препарат, что требует проведения молекулярно-генетических исследований;
- Стоимость веществ, использующихся для таргетной терапии достаточно высока, из-за сложности их получения.
Побочные эффекты
Негативное влияние таргетной терапии на организм гораздо менее выражено, чем в случае использования химиотерапевтических препаратов.
К тому же при использовании данного метода лечения рака в качестве самостоятельного, риск побочных эффектов, способных нести угрозу жизни пациента снижается.
И, тем не менее, при всех плюсах этой новой технологии, побочные реакции все же существуют и могут быть достаточно серьезными, к ним относятся:
- Сыпь и другие проблемы с кожей;
- Расстройства выделительной системы;
- Нарушения в работе центральной нервной системы, эндокринных желез и костного мозга;
- Иногда может возникать артериальная гипертензия;
- Различные нарушения в работе сердечно-сосудистой системы, вплоть до появления сердечной недостаточности;
- Сбои в работе дыхательной системы (могут появиться пневмониты или бронхиолиты);
- Гепатит и иные заболевания печени;
- Расстройство желудка;
- Нарушение функции свертываемости крови, из-за чего порезы и ранки будут заживать медленнее.
Таргетная терапия может вызвать сердечную недостаточность
Эти явления чаще всего встречаются по отдельности и являются гораздо менее выраженными, чем в случае прохождения курса химиотерапии.
Противопоказания
Противопоказания для таргетной терапии похожи на те, которые выдвигаются для химиотерапевтического лечения, с той лишь разницей, что в данном случае вреда пациенту будет нанесено меньше, поэтому таргетная терапия и является хорошим выходом для ослабленных больных.
Таргетная, как и химиотерапия не применяется в следующих случаях:
- Периоды беременности и лактации;
- Детский возраст, вплоть до 18 лет, так как безопасность и эффективность таргетной терапии при применении для детей до сих пор не доказана;
- Повышенная чувствительность к различным компонентам таргетных препаратов.
Источник: https://oonkologii.ru/targetnaya-terapiya-01/
Иммунотаргетная терапия рака желудка
Онкозаболевания – одно из самых сложных направлений медицины. Образовавшиеся злокачественные опухоли иногда удается иссечь хирургически. Но часто операция бывает недостаточна или невозможна. Поэтому наиболее важной составляющей в лечении рака остается лекарственная терапия.
На сегодняшний день активно развивается и внедряется в практику лечения онкобольных такое новое направление терапии, как таргетная терапия. О том, что это такое и в чем ее преимущества, мы поговорим сегодня со старшим научным сотрудником отделения клинической фармакологии и химиотерапии РОНЦ им. Н.Н.
Блохина Минздрава России, доктором медицинских наук Мехти Наримановичем Наримановым.
— Мехти Нариманович, в чем кардинальное отличие таргетной терапии от химиотерапии, которую применяют уже много лет?
Как известно, химиотерапия блокирует рост всех быстроделящихся клеток, что приводит к тяжелым побочным эффектам. Но когда речь идет о смертельном заболевании – выбирать не приходится. Сравнительно недавно (с конца в 90-х годов) появилось новое направление в лекарственной терапии — таргетная терапия.
Это принципиально новый подход к лечению, когда препарат влияет на конкретные (таргетные) мишени, которые участвуют в росте и развитии опухоли. Т.е. действие более локализовано именно на опухолевых клетках.
Зачастую при этом задействуется работа таких противоопухолевых препаратов с иммунными механизмами, этот новый тип таргетной терапии называется иммунотаргетной терапией.
TARGET (англ.) – цель, мишень
— Расскажите немного о том – что же происходит в процессе таргетной терапии? Почему она легче переносится организмом?
Характерное отличие таргетной терапии от основных видов химиотерапии заключается в ее безопасности по отношению к здоровым клеткам организма. К тому же, эта терапия может вызвать быстрое разрушение опухолевых клеток.
Вследствие долгого изучения и осознания процессов образования и жизнедеятельности раковых опухолей разработаны препараты, которые действуют на молекулярные механизмы роста опухолевой клетки.
Опять-таки таргетная терапия – это и самостоятельный вид лечения, и дополнительный к другим методам лекарственной терапии.
На текущий момент все силы биохимических исследовательских центров направлены на получение таргетных медикаментов нового поколения.
Принципиальная разница между классической терапией и лечением инновационными средствами в том, что «умные» лекарства могут четко идентифицировать мутирующие клетки и оказывать разрушающее воздействие исключительно в пределах злокачественного новообразования, не затрагивая при этом здоровых органов и тканей.
Целенаправленное угнетение раковых опухолей – является глобальной целью для такого способа лечения рака. Некоторые препараты влияют на здоровые клетки лишь опосредованно, другие – вовсе игнорируют здоровые макрофаги. Чаще всего таргетная терапия нового поколения используется при лечении рака легких, почки, кожи, желудка, толстой кишки, молочной железы.
— Какие современные таргетные препараты применяются в современной лекарственной терапии опухолей?
Самые популярные и применяемые препараты: «Вотриент», «Нексавар» («Сорафениб»), «Сутент», «Бевацизумаб» («Авастин»), «Эверолимус» («Афинитор»), «Аксинитиб» («Инлита»), Трастузумаб (Герцептин).
В современной лекарственной терапии опухолей их применяют с эффектом и на последних стадиях лечения.
К сожалению, нужно быть готовым к появлению таких негативных проявлений, как повышенное артериальное давление, диарея или усиление чувствительности в конечностях.
— Сколько времени вообще применяется таргетная терапия?
В России уже более 10 лет.
— Но ведь проблема лечения рака в том и состояла, что клетки опухоли аналогичны собственным клеткам организма и собственный иммунитет с ними не справляется. Как же тогда лекарства смогли решить эту проблему?
Известно, что иммунная система позволяет отличать «свое» от «чужого».
В гипотезе выживаемости раковых клеток в собственном иммунитете была представлена теория, согласно которой иммунная система должна находить и истреблять появившиеся злокачественные опухолевые клетки.
Сначала теория эта была отвергнута наукой и медициной, но постепенно в экспериментальных исследованиях были получены весомые доказательства взаимодействия собственного иммунитета человека и иммунотаргетных препаратов.
— Давайте поговорим о препаратах иммунотаргетной терапии для лечения рака желудка. Можете назвать несколько примеров?
Основные препараты на сегодняшний день — «Ниволумаб», «Пембролизумаб», «Авелумаб». Это новейшие препараты иммуннотаргетной терапии. В нашей клинике мы применяем эти препараты в рамках клинических исследований и в рутинной практике.
С этими препаратами проводились клинические исследования при лечении рака желудка и получены неплохие результаты. Но требуются дальнейшие исследования.
Открытие эффективных биомаркеров позволило бы сделать важный шаг в лечении этих групп больных.
— Если рассматривать лечение онкозаболеваний в контексте рака желудка, то, несмотря на прогресс методов лекарственной терапии, прогноз этих больных неблагоприятный. Иммуннотаргетная терапия распространенного рака желудка позволила произвести какие-то сдвиги в этом направлении?
Иммунотаргетная терапия распространенного рака желудка в настоящее время постепенно выходит на передовую позицию. В настоящее время при раке желудка проводится I фаза исследований этого анти-PD-1 иммуностимулирующего антитела самостоятельно или в комбинации.
Предварительные доклинические исследования показали, что двойная блокада РD-1 и СТLА-4 приводила к повышению выброса цитокинов и увеличивала пролиферацию СD8+ и СD4+ Т-клеток по сравнению с блокадой одного из рецепторов.
Исследования по изучению активности Ниволумаба в монотерапии или в комбинации с ипилимумабом у больных метастатическим раком желудка.
Другой иммунотаргетный препарат — Пембролизумаб является высокоспецифичным гуманизированным моноклональным IgG4 антителом, которое блокирует взаимодействие PD-1 c его лигандами PD-L1 и PD-L2.
Недавно было проведено исследование по безопасности и активности пембролизумаба у больных раком желудка в I фазе, в исследование скринировано 165 больных диссеминированным раком желудка.
65 больных были PD-L1 позитивными (критерием служило окрашивание PD-L1 в строме или ≥1% опухолевых клеток), 39 из них получали Пембролизумаб (10 мг/кг) каждые 2 недели. У 41% больных отмечено значительное уменьшение опухоли. Отмечено, что лечение больные перенесли благоприятно.
Важно отметить, большинство иностранных препаратов зарегистрировано в России и входит в бесплатный список жизненно важных препаратов.
— Все эти препараты дорогостоящие и зарубежные?
Да. Большинство этих препаратов разработаны за границей. В основном, это препараты европейские и американские. В России начали делать дженерики некоторых препаратов и они стали более доступными. Важно отметить, большинство иностранных препаратов зарегистрировано в России и входит в бесплатный список жизненно важных препаратов.
- — То есть недостаток – это высокая стоимость?
- Да, недостатком таргетной терапии можно считать высокую стоимость препаратов, обусловленную сложностью их получения, необходимость проводить сложные молекулярно-генетические исследования каждому пациенту для подбора эффективного средства лечения, а также невозможность применения конкретных препаратов у широкого круга пациентов, как это происходит при химиотерапии.
- — Какая примерная стоимость препаратов для таргетной терапии?
В случае приобретения препаратов в аптеках эти препараты дорогостоящие, стоимость их может доходить до 100.000 рублей и более за 1 (один) курс лечения. А курсов может понадобиться 6-8 (шесть-восемь).
— А как обстоят дела в связи с санкциями к нашей стране?
Если это зарегистрированный в России препарат — проблем нет. На них санкции не распространяются. Но если этот препарат еще не зарегистрирован у нас, пациент может сам купить его в Европе и привезти. На границе проблем не должно быть, т.к. у больного есть справка и другие документы, в том числе консилиум врачей, что данный препарат жизненно необходим.
— Получается, что лечение довольно дорогое. Если человек заболевает раком, где он берет препараты?
Как правило, человек становится на учет в онкодиспансере. Могу сказать, что даже во многих региональных онкодиспансерах есть препараты для таргетной терапии.
— В России ОМС покрывает такие расходы?
ОМС — незначительно. Но в России есть система медицинских квот, которая покрывает такие виды дорогостоящей таргетной терапии. Речь о ВМП (высокотехнологичная медицинская помощь).
И здесь иногда удается сделать так, чтобы по квоте покрылись большие суммы.
Консилиум врачей, принимает решение и для данного больного выдают протокол, по которому его госпитализируют для оказания высокотехнологичной медицинской помощи.
— Сколько времени вообще применяется иммунотаргетная терапия рака желудка?
В России и в мире иммунотаргетная терапия является новейшим и самым последним словом в лекарственной терапии рака желудка, и мы надеемся, что уже в течение 3-4 лет мы сами увидим результаты действия этого метода в лечении рака желудка и других опухолей.
Мехти Нариманович, спасибо за интервью! Надеемся, что с Вашей помощью мы смогли в доступной форме рассказать нашим читателям о таком новом методе лечения рака, как таргетная и иммунотаргетная терапия.
Нариманов Мехти Нариманович mehtin@mail.ru +7 (903) 590-06-56 WhatsApp, Viber
Источник: https://Estetmedicina.ru/other/obzory/immunotargetnaya-terapiya-raka-zheludka/
Таргетная терапия в онкологии: препараты для лечения рака
Злокачественная онкология многими воспринимается как приговор, однако в современной медицине постоянно разрабатываются новые методики лечения даже самых сложных заболеваний – таких как рак. В данной статье поговорим об одном из современнейших методов, используемых в его лечении – таргетной терапии, ее применимости, препаратах и стоимости в России и Израиле.
Как и любое новое средство, методика отличается высокой ценой – стоимость препаратов от 15 тысяч рублей за флакон, один курс лечения в израильских клиниках стоит от нескольких тысяч долларов долларов. Более подробно цены рассмотрим в конце статьи.
Данное понятие образовано от английского слова «target» что переводится как «цель». Таргетной терапией называют новейшую разработку, используемую для подавления злокачественных раковых опухолей в онкологии.
Слово «таргетная» означает целевое воздействие только на клетки рака, без нанесения вреда здоровым структурам вокруг и здоровью в целом, что исключает негативные последствия как, например, при химиотерапии или лучевом воздействии.
Такой комплекс лечебных мер показал свою действенность и хорошие отзывы при онкологии почек, легких, молочных желез, меланомы или рака кожи.
К сожалению, степень воздействия на другие опухолевые патологии не отличается высокой эффективностью и применение такого способа неоправданно.
Линейка препаратов, объединенных под названием «таргетная терапия» состоит из ряда лекарственных средств, отличающихся ценой и силой воздействия на разны формы онкологии.
Используя таргетную терапию можно добиться быстрого уничтожения раковых структур. Она родилась после долго изучения процесса развития клеток рака. В результате были получены препараты, точечно воздействующие на центры, обеспечивающие патологический клеточный рост.
На сегодняшний день таргетным называют самостоятельный метод терапии, применяемый как отдельно, так и в комплексе с другими.
Когда показана таргетная терапия
Показаниями для целевого воздействия является:
- Пребывание больного в тяжелом состоянии, когда хирургическое вмешательство или химиотерапия способны сильно ухудшить его положение.
- С целью «разбавления» опасных для здоровых тканей видов терапии.
- Высокий шансы образования метастаз или рецидива удаленной онкологии.
- Агрессивность рака и быстрый рост объема новообразования.
Как действуют препараты
При разработке лекарственных средств они создаются таким образом, чтобы подавлять ДНК и систему рецепторов новообразования. Ввиду этого, оно перестает увеличиваться в размерах, тормозится внутренний прогресс и способность к формированию метастазов.
Благодаря замедлению метастазирования удается значительно улучшить прогноз лечения и срок жизни пациентов, так как главный риск при раке это размножение образования по всему организму.
Мишенями таргетных препаратов выступают:
- Наборы генов, отвечающие за деление и размножение.
- Микроструктуры, контролирующие процессы апотоза или гибели клетки.
- Рецепторы, воспринимающие гормональные вещества в окнкоклетках, что характерно для онкологии молочной железы.
- Сети сосудов, поддерживающие жизнеспособность новообразований.
Обычно таргетное лечение направлено на регресс опухолевого роста и появления метастаз. Благодаря блокировке процесса клеточного деления и остановке кровоснабжения с помощью таргетных препаратов нарушается нормальное развитие опухоли, что постепенно оборачивается ее естественным отмиранием.
Преимущества и недостатки
Несомненное преимущество это целевое воздействие, которым обладает таргетная терапия. «Интеллектуальные» активные вещества препаратов «понимают» какая клеточная ткань здоровая, а какая раковая, и разрушительно действуют только на последнюю.
Целенаправленность дает возможность угнетать развитие злокачественной онкологии легочной системы, почек, груди у женщин естественным путем и без побочных эффектов и последствий.
Главные преимущества
- Препараты имеют форму таблеток
- Минимальные побочные последствия в сочетании с легкой переносимостью
- Высокая эффективность
- Возможность сочетания с другими методами лечения без опасения противопоказаний
Таргетные лекарственные средства имеют форму таблеток, что позволяет их принимать в домашних условиях, не посещая стационар или больницу, как это нужно делать, например, при химиотерапии.
При отсутствии симптомов болезни пациент на протяжении терапии никак не страдает от получаемых лекарств, не падает его работоспособность, что отмечается в отзывах пациентов.
Еще одна важная положительная черта это разграничение препаратов для разных целей. Таргетная терапия при раке может ставить своей целью замедление метастазирования, разрушение иммунных клеточных связей, изоляцию раковых клеток и т.д. Для любой задачи существует свой препарат, который можно быстро включать или выключать из тактики лечения
Минусы таргетной терапии
- Высокая цена, когда стоимость каждого курса начинается от нескольких тысяч долларов.
- Необходимость глубокого молекулярного и генетического обследования для подбора максимально действенного средства.
- Ограниченное воздействие при раке легкого, почек, молочной железы у женщин, меланоме кожи.
Какие используются препараты
На сегодняшний день уже созданы десятки лекарственных средств, относимых к таргетным, которыми успешно лечится рак дыхательной системы, молочной железы, почек, меланома и некоторые другие онкологии. Перечислим наиболее популярные и востребованные препараты:
- Авастин. Служит для разрушения сосудистой питательной сети, что делает невозможным поддержание жизни опухоли. Показал высокий эффект при почечной, легочной и молочножелезистой патологии. Является одним из самых доступных по цене при стоимости за флакон от 15 000 рублей.
- Герцептин. Останавливает опухолевое развитие, воздействуя на факторы данного процесса. Применяется в основном при лечении женщин при новообразованиях в груди, улучшая прогноз на 30-45%, что ведет в большей выживаемости.
- Сорафениб. За счет подавления прогрессирования ракового образования, уходят тяжелые болевые симптомы, и улучшается самочувствие больного.
- Тарцева (Эрлотиниб) эффективен при поражении пищевода, почек, легкого.
Хорошей новостью является быстрое развитие индустрии. Каждый год арсенал таргетной терапии пополняется новыми препаратами, расширяющими диапазон лечимых заболеваний, чем создаются предпосылки для снижения ее стоимости.
Особенности таргетной терапии в онкологии
Рассмотрим подробнее некоторые аспекты и особенности при терапии разных видов рака с помощью таргетного метода.
При раке молочной железы
Онкология груди это опасное женское заболевание. Новейшие исследования позволили получить лекарственные средства, блокирующие эстрогеновые рецепторы, что понижает агрессивность опухоли и ее возможности по формированию метастаз.
Терапию ведут препаратами:
- Торемифеном
- Тамоксифеном
- Фарестоном
- Фазлодексом
- Фулвестрантом
Указанные средства имеют разную стоимость, но у них у всех одна функция – не дать эстрогену соединиться с клетками злокачественной онкологии, из-за чего происходит ее разрастание и миграция.
Следующий этап терапии молочножелезистого рака подразумевает прием медикаментов другого класса, цель которых торможение выработки ароматаза, как называют фермент, принимающий участие в производстве эстрогена. Для этого назначают прием Экземестана, Анастрозола, Аромазина и т.д.
Прием препаратов обоих классов снижает уровень эстрогена, благодаря чему подавляется жизнедеятельность клеток рака.
Улучшает прогноз лечения пребывание женщины в фазе после климакса, когда функционал яичников заметно снижен и секрецию ароматазы заблокировать проще.
При раке почки
При почечной онкологии также существуют эффективные средства таргетной терапии, задача которых не допустить появления сосудистых элементов, ведущих к метастазированию. Лечение ведут следующими таргетными препаратами:
Подобрать конкретное средство может только лечащий онколог. Несмотря на «таргетность» при терапии почки есть некоторые побочные действия, к примеру, рвота, повышение артериального давления выше нормы, дерматит, расстройство кишечника. Однако по сравнению с введением химикатов такие симптомы это сущий пустяк.
При раке легкого
Легочную онкологию сложно обнаружить на ранней стадии из-за слабых симптомов и признаков.
Статистика утверждает, что три четверти заболевавших на момент постановки диагноза неоперабельные.
Для таких людей таргетная терапия это один из немногих шансов приостановить развитие патологического процесса и дать шанс на улучшение прогноза и существующие отзывы это подтверждают.
Механизм действия активных веществ подразумевает остановку прогрессирования роста новообразования с помощью разрушения цепи биологических и химических реакций в нем. Для этого подходят препараты, относящиеся к трем классам:
- Ферментным блокаторам
- Специфическим иммуноглобулинам
- Блокировщикам сосудистого разрастания
Отзывы
Приведем несколько отзывов пациентов, прошедших курс таргетного лечения.
Алена: Рак почек 3 стадии для меня был просто шоком. Слава Богу денежные запасы позволяли лечиться заграницей и я была направлена в израильскую клинику, где мне была проведена таргетная терапия. К тому времени уже было метастазирования, однако вторичные опухоли начали уменьшаться и перестали образовываться новые очаги. В данный момент лечение продолжается, прогноз врачей стал лучше, и я надеюсь на хороший исход.
Светлана: Узнала о таргетной терапии, когда понадобилось проводить химиотерапию. Цена ее гораздо выше, но я решила попробовать, так как очень боюсь побочных действие химического лечения. В данный момент наблюдается ремиссия у метастаз, онкологи успокаивают, что рак перешел из агрессивного течения в спокойное. Пока лечусь и надеюсь на лучшее.
Цена препаратов и стоимость курса таргетной терапии
Стоимость такого лечения не маленькая, особенно на фоне доходов россиян, белорусов, украинцев и т.д. И это сильный ограничитель почему таргетная терапия не получает широкого распространения в этих странах.
Приведем цены на лекарственные таргетные препараты (стоимость одного флакона):
- Авастин – от 15000 руб.
- Герцептин – 32 и более тысяч руб.
- Иматиниб – от 35 тысяч руб.
- Тарцева – от 68 тысяч руб.
Если говорить о стоимости 1 кура таргетной терапии в клиниках, то при лечении в Израиле нужно обладать минимум пятью тысячами долларов. В настоящее время в Москве появляются медицинские учреждения, оказывающие подобные же услуги по цене в 4000 долл.
Источник: http://103med.ru/stati/onkologiya/targetnaya-terapiya
Лечение таргетными препаратами
О таргетных препаратах в онкологии, лечении различных видах опухолей препаратами таргетной терапии рассказывает онколог-химиотерапевт нашей клиники, к.м.н., врач высшей категории Анна Игоревна Буйнякова. За последнее десятилетие в лечении онкологических пациентов был получен значительный прорыв.
Эра химиотерапии претерпела важные изменения. Раньше назначение противоопухолевой терапии основывалось на главных фенотипических характеристиках, таких как: локализация первичной опухоли, гистологический тип и степень ее дифференцировки, общее состояние больного, характер распространения опухолевого процесса и т.
д.
К существенным недостаткам химиотерапии следует отнести ограниченную эффективность цитостатиков; диапазон их активности колеблется от 20 до 80%.
Максимальная эффективность наблюдается у ограниченной группы препаратов, таких как Таксаны, производные и препараты Платины. Поэтому сегодня в помощь врачу и пациенту есть препараты таргетной терапии.
В современной онкологии без знания молекулярно-генетических характеристик опухоли не обойтись.
Оно позволяет индивидуализировать лечение и улучшить качество жизни, а по некоторым нозологическим формам значительно увеличить ее продолжительность.
И речь идет не о месяцах, а о годах, отвоеванных у болезни. Лечение таргетными препаратами обладает принципиально иными механизмами воздействия на опухоль.
Большинство рецепторов в опухоли – это факторы роста, представленные тирозинкиназными рецепторами, каждый из которых имеет экстрацеллюлярную часть — часть вне клетки, ответственную за соединение с фактором роста или другим лигандом — рецептором, трансмембранную часть (в толще стенки клетки) и интрацеллюлярную часть (в глубине клетки), представленную ферментом тирозинкиназой С. На все эти части рецептора в той или иной форме воздействуют таргетные препараты, блокируя или разрушая их. Так погибает опухолевая клетка. Выключение функции рецептора возможно за счет блокирования экстрацеллюлярной части рецептора моноклональными антителами или ингибирования активности тирозинкиназы С.
Пришло время признать, что таргетные препараты в онкологии как в монорежиме, так и в комбинации с химиотерапией могут обладать высокой противоопухолевой активностью.
Но наряду с этим нормальные ткани также могут экспрессировать аналогичные рецепторы, в связи с чем может наблюдаться ряд побочных эффектов, отличных от наблюдаемых при стандартной химиотерапии. Но этого не стоит бояться, так как все побочные эффекты лечения известны, тщательно изучены и успешно корректируются либо снижением дозы, либо индивидуальным назначением симптоматической терапии.
Некоторое таргетные препараты при раке выпускаются в таблетированной форме, что очень удобно для применения на дому и для коррекции дозировки с целью контроля побочных реакций.
Источник: https://cpm-devita.ru/hospital/targetedtherapy/preparaty/

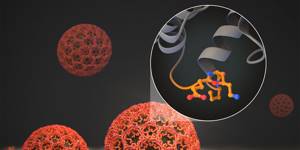
 — Мехти Нариманович, в чем кардинальное отличие таргетной терапии от химиотерапии, которую применяют уже много лет?
— Мехти Нариманович, в чем кардинальное отличие таргетной терапии от химиотерапии, которую применяют уже много лет?  Большинство рецепторов в опухоли – это факторы роста, представленные тирозинкиназными рецепторами, каждый из которых имеет экстрацеллюлярную часть — часть вне клетки, ответственную за соединение с фактором роста или другим лигандом — рецептором, трансмембранную часть (в толще стенки клетки) и интрацеллюлярную часть (в глубине клетки), представленную ферментом тирозинкиназой С. На все эти части рецептора в той или иной форме воздействуют таргетные препараты, блокируя или разрушая их. Так погибает опухолевая клетка. Выключение функции рецептора возможно за счет блокирования экстрацеллюлярной части рецептора моноклональными антителами или ингибирования активности тирозинкиназы С.
Большинство рецепторов в опухоли – это факторы роста, представленные тирозинкиназными рецепторами, каждый из которых имеет экстрацеллюлярную часть — часть вне клетки, ответственную за соединение с фактором роста или другим лигандом — рецептором, трансмембранную часть (в толще стенки клетки) и интрацеллюлярную часть (в глубине клетки), представленную ферментом тирозинкиназой С. На все эти части рецептора в той или иной форме воздействуют таргетные препараты, блокируя или разрушая их. Так погибает опухолевая клетка. Выключение функции рецептора возможно за счет блокирования экстрацеллюлярной части рецептора моноклональными антителами или ингибирования активности тирозинкиназы С.