Канцероматоз брюшной полости представляет собой вторичное онкологическое образование. Клетки опухолей метастазируют из других очагов поражения.
Согласно медицинской статистике, узнать, что такое канцероматоз брюшной полости, приходиться 35% пациентам с онкологией. В большинстве случаев это люди, с раковыми образованиями в органах желудочно-кишечного тракта и яичников.
Последнее говорит о том, что женская половина подвержена патологии больше мужской.
Признаки и классификация
Из-за вторичности заболевания, изначально у человека присутствуют первичные симптомы рака в виде боли и нарушенного пищеварения. Одним из признаков канцероматоза и чаще всего единственным является асцит брюшины, что это такое пациенты узнают при осложнении онкологии органов и циррозе.
Заболевание проявляет себя скоплением жидкости в животе, давящей на органы. Исходя из статистики, каждый третий пациент умирает от водянки. При наличии больших метастаз, врач может их прощупать.
В стационар человек при
канцероматозе поступает в тяжелом состоянии, у него увеличен живот,
наблюдается:
- потеря веса;
- тошнота, рвота;
- головная боль;
- низкая или
высокая температура; - вялость.
Канцероматоз брюшной полости входит в международный класс мкб 10. Целью классифицирования является сбор статистики данных о ситуации со здоровьем групп населения, подсчете смертности и влиянии различных факторов.
Причины возникновения
Концероматоз брюшной
полости вызывает распространение раковых клеток от других органов, что
происходит через лимфатическую и кровеносною систему или после операции по удалению первичной опухоли.
Стремительному распространению способствует:
- Тесный контакт брюшины с пищеварительными органами.
- Соприкосновение складок живота друг с другом.
- Внушительное количество лимфоузлов и кровеносных сосудов в области.
Методы мсследования
Диагностировать заболевание врач начинает с изучения анамнеза, симптомов, и после сдачи анализов. При подозрениях на канцероматоз, пациенту назначают аппаратное исследование, оно помогает выявить расположение новообразования, оценить состояние брюшной полости.
Компьютерная томография
Эффективные методы диагностики также включают в себя:
- компьютерную томографию;
- цитологическое исследование жидкости;
- анализ крови ОТ-ПЦР;
- лапароскопию;
- МСКТ.
В 3-5% ситуаций размеры первичного образования настолько
малы, что затрудняют диагностику или не выявляются. В таких случаях клиника
канцероматоза брюшной полости наблюдается уже при обширном поражении, что
делает лечение неэффективным, а состояние пациента контролируют паллиативной
терапией.
Медицинская помощь
Лечение канцероматоза брюшной полости длительное и сложное. Медикам приходится бороться за жизнь пациента. К больному применяют химиотерапию, делают операцию, снимают острые симптомы. Дополнить лечение канцероматоза можно нетрадиционной медициной, несмотря на то что, она не доказана научно, сами врачи рекомендуют некоторые рецепты, но только в комплексе с основной терапией.
Хирургическое лечение
Операция проводится в случаях, если позволяет стадия канцеромотоза и локализация поражения. Она направлена на иссечение первичной опухоли, поврежденных лимфатических узлов, метастаз в области живота.
Так как первичные очаги раковых клеток при канцероматозе в большинстве случаев образуются в пищеварительных органах и яичниках, хирурги могут удалить желчный пузырь, сигмовидную кишку, доли толстого или тонкого кишечника, матку, придатки.
Химиотерапия
Прогноз для пациентов 4 степени канцероматоза неутешителен. Операцию в таких случаях не проводят, лечат обычной химиотерапией, снимают симптомы, при асците удаляют жидкость.
В современных клиниках, введение лекарств осуществляют посредством горячего воздуха в пораженную область. На ранних стадиях канцероматоза брюшной полости, процедуру можно осуществить в процессе оперативного вмешательства.
При таком способе, жидкость убивает онкологические клетки на протяжении 60 минут, в дальнейшем усиливает эффективность лечения.
Симптоматическая терапияН
Чтоб облегчить жизнь больному, задача врачей – снять клинику канцероматоза брюшной области и асцита, для этого прибегают к следующим методам:
- Прокалывают
область живота, чтоб выпустить скопившуюся воду. - Сильные
боли притупляют путем инъекций с наркотическим анальгетиком. - Интоксикацию
снимают капельницами. - Для
вывода жидкости также используют мочегонные препараты (Фурациллин).
Народные средства
Перед тем как использовать народные методы лечения канцероматоза брюшной полости, врачи настоятельно рекомендуют обсудить рецепты, в противном случае можно усугубить ситуацию и уменьшить продолжительность жизни. Опасения связаны с индивидуальностью каждого человека, сопутствующими заболеваниями, противопоказаниями, возможными осложнениями и отравлениями после употребления составов.
Чаще всего в составе противораковых рецептов преобладают:
- пижма;
- полынь;
- сабельник;
- сныть;
- ромашка;
- мята;
- подорожник;
- чистотел;
- тысячелистник и другие.
На основе трав готовят отвары и настои, в отсутствии противопоказаний составы можно употреблять в целях профилактики. При канцероматозе брюшной области эффективны следующие рецепты.
Пеларгония с коньяком
Для этого рецепта при канцероматозе необходимо 2 листа пеларгонии, которые заливают 50 мл кипятка и настаивают сутки в термосе. Полученную жидкость соединяют с 500 мл конька, 3 суповыми ложками сока алое, 2 каплями йода. Лекарство пьют с утра и перед сном.
Настойка болиголова
Растение ядовитое, поэтому важно соблюдать дозировку. Лекарство можно купить в готовом виде или сделать самостоятельно.
В приготовлении понадобиться 0,5 л спирта и 50 г сухого болиголова, которые ставят на 14 дней в темное место и регулярно перемешивают.
ИЗОБРАЖЕНИЕ одно или два 660*(100-420) Средство при канцероматозе употребляют: 4 дня подряд по 1 капле, 4 раза в сутки; с 5 по 8 день количество капель 2; на 9 день 3 капли;на 10 сутки 4 капли; на 11 день 5 капель. Готовую настойку пьют при канцеромотозе по 2 капли перед приемом пищи в 1 сутки, на следующий день 3 капли.
Количество капель увеличивают на 1 каждый день, пока не дойдут до 20, после чего прием идет в обратном порядке на уменьшение. Закончив курс, организму дают время на отдых, через 2 недели схему повторяют. В год разрешено не более 3 курсов.
Настой картофельных цветов
В лечении канцероматоза эффективны соцветия картофеля. Собранные цветы высушивают без воздействия солнца. Смесь в количестве 2 горстей заливают 0,5 л спирта и оставляют на 2 недели в темном месте. Далее жидкость процеживают, разводят в пропорции 7 капель на 50 мл воды и пьют 3 раза в сутки.
Травяной сбор №1
Для лекарства от канцеромотоза нужны почки черного тополя в количестве 5 г, аир 8 г, 25 г соцветий лопуха и 35 г корня, цветы полевого бодяка 50 г. Смесь заливают 0,9 мл кипятка, настаивают и пьют перед едой, разделив на 3 суточных приема.
Травяной сбор №2
Следующий рецепт при канцероматозе включает экстракты чаги и столетника по 200 г, шиповник, тысячелистник, сосновые шишки по 50 г, полынь 5 г, коньяк 250 г, мед 500 г. Ингредиенты заливают 3 литрами кипятка, варят 2 часа, настаивают сутки, употребляют по 1 большой ложке перед приемами пищи на протяжении 2 недель.
Настойка полыни
Трава хорошо зарекомендовала себя в лечении онкологии, на ее основе делается одно из противораковых лекарство Артемизинин. При канцероматозе можно пить аптечную настойку полыни в количестве 15 капель, не более 3 раз в сутки, курсом 14 дней.
Настойка одуванчика
Корни растения промывают и оставляют обсыхать, используют после прекращения выделения молока. Траву подсушивают при температуре 40-50 градусов, берут в количестве 3 суповых ложек, заливают 500 мл кипятка, варят на медленном огне 20 минут. Процеженную жидкость употребляют при канцероматозе после еды, 2 раза в день по 250 мл.
Продолжительность и прогноз жизни
Канцероматоз брюшной полости имеет неблагоприятный прогноз жизни, учитывая, что заболевание – это уже метостазы, а его симптомы обычно проявляются, когда клетки достаточно распространились.
https://www.youtube.com/watch?v=7TlAp79fkjk
Продолжительность жизни пациентов при канцероматозе брюшной полости 4 степени менее 12 месяцев, начальные стадии имеют прогноз 5-летней выживаемости 10%, таким образом, сколько точно живут пациенты, определяет своевременная диагностика и лечение.
Что такое канцероматоз брюшной полости, прогноз жизни и сколько живут при 4 степени Ссылка на основную публикацию
Источник: https://OtekOff.ru/otek/otek-zhivota/kantseromatoz-bryushnoj-polosti
Канцероматоз брюшины: продолжительность жизни, фото, лечение, признаки и причины
Злокачественные новообразования практически любых органов приводят к появлению метастазов. Вторичные очаги значительно уменьшают шансы больного на полное выздоровление.
К метастазам относят и канцероматоз брюшины, проявляющийся в основном асцитом, нарастающими симптомами интоксикации и снижением веса. Канцероматоз считается крайне неблагоприятным по течению заболеванием, при таком осложнении в основном используется паллиативная, то есть поддерживающая жизнь терапия.
Что такое канцероматоз брюшины?
Канцероматоз – онкологическая, вторичная патология являющаяся следствием переноса раковых клеток из первичного очага.
Перенос в большинстве случаев осуществляется посредством лимфосистемы, реже кацероматоз обуславливается прорастанием первичной злокачественной опухоли в брюшину.
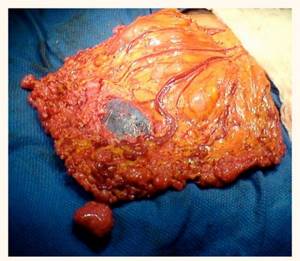
Попавшие в серозные полости раковые клетки закрепляются в них и начинают формировать образования, по форме они напоминают зерна проса. Постепенно эти новообразования расширяются в размерах, занимают все новые площади и в итоге сливаются между собой, создавая большую опухоль.
На фото показан вскрытый канцероматоз брюшины
Злокачественный процесс приводит к тому, что нарушается резорбтивная и экссудативная функции серозной оболочки брюшины. Подобное изменение становится причиной скопления избыточной жидкости, которая накапливается и приводит к асциту.
Обследование пациентов с канцероматозом брюшины позволило выяснить, что данное осложнение чаще всего встречается у больных с раком органов желудочно-кишечного тракта – желудка, поджелудочной железы.
На втором месте среди причин возникновения канцероматоза стоит рак яичников, что указывает на то, что женщины этому осложнению подвержены в несколько раз больше по сравнению с мужчинами.
Поражение брюшины при раке любого из органов считается неблагоприятным признаком. Многие виды лечения при таком диагнозе использовать невозможно, поэтому пациент не живет долго.
Причины возникновения
Основная причина формирования канцероматоза брюшины это уже имеющийся первичный раковый очаг. Опухолевые клетки неизбежно в результате своего развития приобретают подвижность, и таким образом могут отделяться и передвигаться.
Их распространение происходит:
- С током крови или лимфы.
- Путем прорастания первичного злокачественного новообразования в брюшину.
- При хирургическом вмешательстве, предпринятом по поводу удаления первичной раковой опухоли.
Площадь брюшины и соответственно серозной оболочки, куда могут попасть опухолевые клетки, достигает у некоторых людей двух квадратных метров. Подобные размеры определяют и расположение брюшины в брюшной полости, то есть она имеет соприкасающиеся друг с другом складки.
Такое анатомическое строение способствует тому, что при злокачественном процессе поражается сразу значительная часть брюшины.
Быстрому развитию канцероматоза способствуют несколько провоцирующих болезнь факторов, это:
- Тесное соприкосновение брюшины с большей частью органов пищеварения.
- Постоянное плотное соприкосновение складок брюшины друг с другом.
- Наличие обширной сети лимфатических и кровеносных сосудов в органе.
Раковые клетки, попавшие в брюшину, стараются закрепиться там, где орган меньше всего подвержен влиянию перистальтики кишечника. Вероятность канцероматоза зависит также от размеров первичной опухоли, степени ее проникновения вглубь органа.
При недифференцированном раке желудка брюшина поражается опухолевыми клетками у большей половины больных.
Признаки и классификация
Но в некоторых случаях именно поражение серозной оболочки с соответствующей клинической картиной позволяет выставить диагноз рака.
К основным признакам, указывающим на развитие злокачественного поражения брюшины, относят:
- Появление тупых, ноющих болей. Они могут быть как постоянными, так и беспокоящими больного периодами по несколько часов или дней.
- Увеличение живота на фоне резкого снижения веса. Увеличивающийся в размерах живот образуется по причине скопления в брюшной полости жидкости, данная патология обозначается термином асцит.
- Выраженное нарушение пищеварения. У больного появляется тошнота, боли и колики в животе, возможна рвота. Возникают трудности с опорожнением кишечника, нередко запор сменяется поносом.
- Усиливающиеся симптомы интоксикации. Сильная слабость, проливные поты, озноб, повышение температуры, боли в мышцах и голове – все эти признаки характерны для развивающегося канцероматоза брюшины.
Общее состояние больного тяжелое, нередко такие пациенты попадают в хирургию или гастроэнтерологию с диагнозом асцит, основная причина которого выясняется позже.
В медицине используется классификация канцероматоза брюшины, основанная на локализации метастазов и их числе:
- Р1 – это локальное, то есть ограниченное одним участком поражение брюшины.
- Р2 – выявление несколько очагов, указывающих на кацероматоз. Между этими очагами имеются участки неизмененной брюшины.
- Р3 – многочисленные, сливающиеся между собой злокачественные очаги.
Диагностические меры
- Заподозрить канцероматоз брюшины по симптомам онколог в первую очередь может уже у тех людей, которые в анамнезе имеют т раковое заболевание.
- Но в любом случае при неясных болях в животе, снижении веса и других признаках ракового образования врач обязан для подтверждения или исключения диагноза отправить своего пациента на ряд диагностических процедур.
- Назначается:
- УЗИ органов брюшной полости, органов малого таза. Этот метод позволяет обнаружить локализацию первичной опухоли, выявляет изменения в брюшине, их расположение, размеры.
- Компьютерная томография исследует брюшную область послойно, выявляя все патологические очаги, их структуру, место расположения.
- МСКТ с контрастом необходимо для оценки распространенности опухолевого процесса, обнаружения поражений лимфоузлов.
- Лапароскопия позволяет не только осмотреть брюшину, но и забирает измененные ткани для проведения биопсии.
- Анализ крови ОТ-ПЦР устанавливает с высоким процентом точности место локализации первичного очага.
Примерно в 5% случаев сложности возникают при выявлении первичной раковой опухоли, иногда ее размеры настолько минимальны, что прижизненно обнаружить ее не удается.
Медицинская помощь
При возможности назначается хирургическая операция, сочетаемая с химиотерапией.
Используется и много новых методик противоракового лечения, поэтому нельзя сказать, что в будущем не будет найден способ победы над злокачественным поражением брюшины.
Хирургическое лечение
Хирургическое лечение заключается прежде всего в удалении первичного очага, пораженных лимфоузлов и очагов осеменения опухолевыми клетками в брюшине. Операция часто сочетается с одновременным удалением матки и ее придатков, желчного пузыря, сигмовидной кишки, части толстого или тонкого кишечника.
Химиотерапия
При лечении пациентов с канцероматозом брюшины сейчас используют один из современных методов – интраперитонеальную гипертермическую химиотерапию. Заключается этот способ во введении химиопрепаратов при помощи горячего воздуха непосредственно в брюшину, что возможно сразу во время операции.
Раствор с химиопрепаратами находится в брюшине около одного часа, за это время он непрерывно циркулирует и уничтожает раковые клетки. Гипертермическая химиотерапия повышает эффективность лечения в несколько раз.
Лечение первичного очага
При канцероматозе брюшины необходимо обнаружить первичный очаг и оценить его стадию, локализацию, распространенность метастазов по организму. Решение о лечении принимается после всех исследований.
Если стадия ракового процесса и место расположения опухоли позволяет, то проводится операция по удалению новообразования. Дополнительно назначаются сеансы химиотерапии, лучевого облучения.
Симптоматическая терапия
Симптоматическая терапия это лечение, направленное на устранение или снижение основных симптомов болезни. При канцероматозе чаще всего проводят:
- Лечение асцита. Заключается оно в удалении скопившейся жидкости через прокол в брюшной стенке.
- Обезболивание, в запущенных случаях снять боль помогает только наркотический анальгетик.
- Улучшение работы органов пищеварения. Необходимо усилить перистальтику, улучшить переваривание и усвояемость пищи.
- Внутривенное вливание растворов. Подобное лечение обладает дезинтоксикационным воздействием и нормализует электролитный состав крови.
- Лечение мочегонными препаратами, которые способствуют выводу излишней жидкости.
При необходимости больным назначаются препараты для улучшения работы сердца и сосудов, ферменты, спазмолитики. Больной обязательно находится под наблюдением с периодическим повторным диагностическим осмотром.
Продолжительность и прогноз жизни
Выявление канцероматоза брюшины у пациентов с раковыми новообразованиями значительно ухудшает прогноз их жизни.
Если задета небольшая часть брюшины, которую можно удалить, то все заканчивается относительно благоприятно, то есть больной может жить несколько лет. Но также прогноз жизни зависит и от того поддается ли лечению первичный очаг.
Если канцероматоз захватывает большую часть брюшины, то смерть пациента наступает за несколько месяцев. Паллиативная медицина позволяет лишь несколько облегчить его самочувствие.
Источник: http://gidmed.com/onkologiya/oslozhneniya/kantseromatoz-bryushiny.html
Эффективное лечение рака 4 стадии (метастазы, канцероматоз, асцит)
LHIPEC – новое в лечении рака органов брюшной полости 4 стадии: рак желудка, рак кишечника, рак яичников.
Данный материал подготовлен медицинским координатором нашего центра и врачами – онкологами из Новосибирска и Владивостока в результате медицинской стажировки в Корею (30.09 – 05.10.2022) в клинику СЭМ на изучение современного метода LHIPEC для лечения пациентов с диагнозом: рак желудка, рак кишечника, рак яичников 3 и 4 стадии, с метастазами в брюшной полости, асцитом и канцероматозом.
В данной статье также использована информация из зарубежных научных исследований и публикаций, предоставленных доктором Ли, онкологом, главврачом клиники СЭМ, Корея, и практикующим хирургом по методике LHIPEC.
Метастазы в брюшной полости.
Это вторичные злокачественные образования, источником которых стала первичная опухоль, могут образовываться в лимфоузлах, в соседних и даже отдаленных органах, в костях. Метастазы разделяют на одиночные, множественные, мелкие и крупные, опасные и менее опасные.
Канцероматоз.
Канцероматоз брюшины – это метастатическое поражение стенок брюшной полости и поверхностей тканей органов.
Как правило, канцероматоз – это признак 3 или 4 стадии рака, чаще терминальной, то есть заключительной стадии развития онкологии.
Обычно это множественное поражение тканей, в виде белых бугристых плотных образований. Далее мы расскажем, как эти образования меняются после проведения операции LHIPEC.
Асцит.
Асцит в брюшной полости – это свободная жидкость, которая появляется в результате прогрессирования онкологии (важно, чаще асцит является следствием цирроза печени, реже – онкологии). Жидкость скапливается в брюшине, ее может быть мало, а может быть несколько литров. При онкологии жидкость содержит в себе атипичные (злокачественные) клетки.
Спайки.
Мало кто обращает внимание из пациентов на данный фактор, но спайки – опасная проблема для пациента. Дело в том, что ткани нашей брюшной полости имеют так называемый слипчивый характер.
При перенесенных операциях, закрытых травмах живота, лучевой терапии может происходить «склеивание» органов между собой или со стенками брюшины.
Само склеивание выглядит как белые фиброзные ткани разной плотности и длины, крепко соединяющие органы и стенки брюшины там, где этого не должно быть. Такой процесс может привести даже к летальному исходу как одно из осложнений лечения.
Если диагноз онкология поставлен, то в зависимости от условий, назначают операцию, химиотерапию, лучевую терапию. Современные способы лечения рака сегодня также включают иммунотерапию, таргетную терапию, криоабляцию, гипертермию и многое другое.
Удивительно, но иногда именно смешение типов лечения дает совершенно новый результат и прорыв в лечение рака, особенно при последних стадиях. Именно так появилась методика LHIPEC.
Разберемся по порядку.
- Есть обычная химиотерапия. Для каждого вида рака – свой протокол, часто даже несколько, если первая линия не помогла или у пациента развилась химиорезистентность, то есть привыкание к данному препарату, назначают другой протокол.
- Есть обычная операция, хирургическое удаление образования. Операция бывает лапароскопической (малоинвазивное вмешательство через 2-3 прокола с использованием эндоскопического оборудования) и лапаротомическая, то есть с открытым доступом.
- Есть гипертермия. Это нагревание того места пациента, где локализуется опухоль, как бы «прогревание» до 44-45 градусов. Данный метод используют для усиления эффекта от лечения химиотерапией или лучевой терапией, так как высокая температура пагубно сказывается на злокачественных клетках, в то время как здоровые клетки способны ее выдержать.
Сначала получилась открытая операция с применением HIPEC: после удаления образования и возможно лимфоузлов, пациенту в течение 40 минут промывают брюшную полость химиопрепаратом, подогретым до 39 градусов, после чего сшивают место доступа и заканчивают операцию.
The New England Journal of Medicine, 18 января 2018. Группа ученых и онкологов Голландии и Дании. Публикация результатов клинических испытаний применения HIPEC.
- 245 пациентов с раком яичников 3 стадии (1 группа 123 чел. без и 2 группа 122 чел. с HIPEC)
- Клинические испытания длились с апреля 2007 по апрель 2016 годов
- 3 курса неоадъювантной (до операционной) химиотерапии (карбоплатин + пакситаксел)
- Оперативное удаление образования
- Внутрибрюшинная гипертермическая химиотерапия в конце операции (цисплатин)
Результаты исследования:
Средняя продолжительность ремиссии без рецидива рака:
- 1 группа = 10,7 месяцев
- 2 группа = 14, 2 месяца
Средняя выживаемость пациентов в течение 4,7 лет наблюдения:
- 1 группа = 38 %
- 2 группа = 50 %
Обратиться в клинику
Исследования метода «горячей» химиотерапии во время операции показали, что этот метод может быть очень эффективным в вопросе продления жизни пациента с раком органов брюшной полости на 3 и 4 стадиях, и даже позволяет добиться большего процента пятилетней выживаемости пациентов с тяжелой степенью рака.
Единственная проблема: этот метод применим один раз, во время открытой операции. Как только ученые и врачи это поняли, начался следующий этап исследований: сделать эту процедуру повторной, для усиления эффективности лечения рака.
Так появился метод LHIPEC – лапароскопическая внутрибрюшинная гипертермическая химиотерапия. Это смешение тех же методов: химиотерапия, операция и гипертермия, только в данной случае малоинвазивная операция, через 2-3 прокола с помощью эндоскопов, что позволяет повторять процедуру несколько раз (от 2 до 10) с интервалом 3-4 недели.
LHIPEC позволяет локально воздействовать на опухоль, метастазы, канцероматоз, избавиться от асцита и запустить процесс уничтожения атипичных клеток. В отличие от системной химиотерапии, которая при 4 стадии рака помогает лишь поддерживать состояние больного, но не лечить.
На сегодня, пожалуй, это единственное средство лечения рака желудка, рака кишечника, рака яичников и других (список ниже в таблице), которое позволяет эффективно избавиться от продуцирования асцита, от канцероматоза и метастаз в брюшной полости.
Описание процедуры
LHIPEC – это оперативное вмешательство, осуществляется под общим наркозом, средняя продолжительность операции около 1,5 – 2 часов. В области брюшной полости хирург делает 2-3 прокола для введения камеры и одного или двух эндоскопов, с помощью которых он сможет:
- откачать асцит,
- взять жидкость на анализ,
- взять образец ткани из канцероматозного образования брюшной стенки,
- по возможности разделить спайки для нормальной циркуляции последующей химиотерапии и максимального доступа ко всей пораженной площади в брюшной полости.
Это все называется ревизия брюшной полости. При этом опытный хирург оценивает общий объем поражения брюшной полости по специальной шкале PCI, считает количество откаченной жидкости, оценивает состояние плотности и жизнеспособности канцероматозных тканей и спаечных тканей.
По окончании всех процедур устанавливаются трубки вместо эндоскопов и подключается аппарат для промывания брюшной полости химиотерапией.
Подобранный под диагноз препарат или комбинация препаратов подогревается до 41-42 градусов по Цельсию, поступает в брюшную полость, циркулирует и откачивается через другую трубку уже с температурой 39-40 градусов.
Процедура длится около 60-90 минут в зависимости от состояния пациента, после чего откачивается вся возможная свободная жидкость, оборудование снимается, накладываются швы.
Назначение метода:
Данный метод назначается пациентам при условии наличия метастаз в брюшной полости, канцероматоза и асцита. В основном, наиболее сильный эффект проявляется у пациентов с диагнозом рак желудка, рак кишечника, рак яичников, мезотелиома. Реже под условия участия попадали пациенты с диагнозом рак матки, рак поджелудочной железы, рак желчного пузыря.
Частота применения:
LHIPEC проводят от 1 до 10 раз. Все зависит от диагноза, от стадии рака, от состояния брюшной полости и самого пациента, от подобранных препаратов и ответной реакции организма. Ниже в таблице приведены данные по количеству раз и эффективности.
Обратиться в клинику
Результаты клинических испытаний клиники G SAM Hospital, Korea, доктор Chaiyoung Lee, частота применения:
| Количество раз LHIPEC | |||||||||||
| Количество пациентов Виды рака |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | Всего раз |
| Рак желудка | 262 | 109 | 50 | 29 | 15 | 10 | 6 | 3 | 1 | 1 | 486 |
| Рак яичников | 84 | 42 | 19 | 13 | 7 | 4 | 3 | 172 | |||
| Рак кишечника | 72 | 26 | 12 | 6 | 3 | 1 | 1 | 121 | |||
| Рак поджелудочной железы | 33 | 7 | 2 | 1 | 1 | 1 | 1 | 1 | 47 | ||
| Рак желчного пузыря | 30 | 8 | 3 | 2 | 2 | 2 | 1 | 1 | 49 | ||
| Аденокарцинома неуточненной локализации | 25 | 12 | 8 | 1 | 46 | ||||||
| Мезотелиома | 18 | 13 | 7 | 7 | 5 | 5 | 3 | 3 | 2 | 1 | 64 |
| Рак матки | 7 | 3 | 1 | 1 | 1 | 1 | 1 | 15 | |||
| Другие виды | 22 | 5 | 2 | 29 | |||||||
| Всего пациентов / раз | 553 | 225 | 104 | 60 | 34 | 24 | 16 | 8 | 3 | 2 | 1029 |
Во время стажировки мы присутствовали на трех операциях. Первой была пациентка с раком яичников 4 стадии, LHIPEC проводился ей впервые.
Во время ревизии брюшной полости благодаря введенной камере было видно, насколько сильно поражена брюшная полость: ткани воспаленные, канцероматозные образования по всем стенкам брюшины и на поверхности органов, асцит около 2,5 литров, жесткие плотные спайки, которые можно было только рассечь, что опасно, так как во многих местах они проросли рядом с сосудами.
Далее была операция у пациентки тоже с раком яичников второй стадии. Но ей LHIPEC проводили уже второй раз. И мы отчетливо увидели процессы разложения злокачественных образований, канцероматозные ткани были пожелтевшими (некроз), плоскими, в меньшем объёме и количестве (со слов хирурга по сравнению с первой операцией), асцит накопился за 4 недели всего около 800 мл.
, а спайки стали мягкими и рыхлыми, хирург легко их разделял даже камерой. То же самое мы увидели на повторной процедуре LHIPEC у пациента с раком желудка на 4 стадии. Эффект воздействия локальной горячей химиотерапии был очевиден.
«Эффект от использования Лапароскопической перитонеальной гипертермической химиотерапии у пациентов с перитонеальным метастатическим раком органов ЖКТ»
- Участники проекта: Доктор Chaiyoung Lee, доктора и ученые из Японии, Кореи и Китая.
- Срок проведения клинических испытаний 2008 – 2014 года.
Данные о результатах исследований:
| Показатели | Рак желудка | Рак кишечника |
| Уменьшение объема асцита | 72% | 79% |
| Уменьшение показателя PCI (объема поражения) | 61% | 65% |
| Увеличение средней продолжительности жизни до | 11,5 мес | 20,8 мес |
| Обычная средняя продолжительность жизни без LHIPEC | 3,1 месяц | 5,2 месяца |
*Данные опубликованы Cancer&Clinical Oncology. Vol.3 No.2; 2014
Михаил К., 50 лет. Новосибирск.
Обратилась супруга Михаила. Пациент с аденокарциномой желудка 4 стадии, после оперативного удаления опухоли, 6 курсов полихимии, 3 монокурсов таргетной химии. На момент обращения сохранялся канцероматоз и небольшой объем асцита, метастазы в брюшной полости.
При рассмотрении данного запроса, доктор Ли предложил следующую схему лечения. Пациент заканчивает курс химии, вместо следующего курса через 3 недели приезжает в Корею на проведение процедуры LHIPEC. Затем на Родине через 3 неделе делает следующий курс химиотерапии, после чего снова приезжает в Корею на вторую процедуру через 3 недели.
По окончании лечения по данной схеме в Корее пациенту провели контрольное обследование, которое показало полное отсутствие метастаз, канцероматоза и асцита в брюшной полости. Согласно протоколу лечения, пациент продолжает принимать таргетный препарат на снижение риска рецидива заболевания.
Эффективное лечение рака 4 стадии есть. Благодаря таким методам как LHIPEC, у пациентов появляется шанс. Этот метод позволяет убрать острое состояние у пациента, дает время общему системному лечению подействовать и быть более эффективным, дает больше времени качественной жизни и больший процент выхода в длительную ремиссию.
Выезд на период 10-12 дней с учетом предоперационного обследования.
Предоперационные обследования – от 500 до 1500 USD (около 32 000 – 96 000 рублей).
Процедура LHIPEC – от 8 000 до 10 000 USD (около 515 000 – 640 000 рублей), зависит от препарата химиотерапии.
Авиа билет до Сеула и обратно.
Питание.
Отправляйте ваши медицинские документы (копии) и снимки в электронном виде на почту info@med-core.com.
Запрос врачу обрабатывается бесплатно, в течение 2-3 рабочих дней.
Если доктор Ли считает, что данному пациенту можно помочь методом LHIPEC, он дает план лечения, мы его вам пришлем сразу по получении, с указанием нужных сроков выезда и необходимого бюджета.
В случае выезда, вас ведет медицинский координатор нашего центра, начиная с подготовки к выезду, во время нахождения в клинике и после возвращения по программе пост-сопровождения.
Обратиться в клинику
Источник: https://med-core.com/effektivnoe-lechenie-raka-4-stadii/
Канцероматоз брюшины при раке: что это такое, симптомы, причины канцероматоза брюшной полости, прогноз
Канцероматоз брюшины — опухолевое поражение листков слизистой оболочки, покрывающей органы и внутреннюю стенку живота. Преимущественно обусловлен разрастанием метастазов рака в брюшной полости, иногда возможно развитие первичного злокачественного процесса — мезотелиомы в самой брюшине.
Метастатическое поражение правильнее называть «карциноматоз», поскольку карцинома — синоним рака. Аналогично метастазы саркомы в брюшину именуют «саркоматоз».
Частое, но не обязательное проявление перитонеального канцероматоза — выработка асцитической жидкости. С асцитом или без, но поражение брюшины злокачественным процессом всегда угрожает жизни больного и требует очень непростого лечения.
Причины канцероматоза брюшины
Не всякая оторвавшаяся от материнской раковой опухоли клетка способна стать метастазом, в кровеносном русле погибает львиная доля циркулирующих злокачественных клеток. Для обретения способности стать метастазом раковая клетка должна измениться внутренне — научиться вырабатывать вещества, позволяющие самостоятельно жить и внедриться в другом месте, подавляя нормальные клетки.
Оторвавшиеся от узла клетки мигрируют на большие расстояния, раздвигая нормальные клетки, имплантируются в брюшную слизистую, способны даже внедряться внутрь других клеток. После закрепления на местности, начинается размножение и образование целой клеточной колонии.
Кроме переноса метастатических клеток по крови и лимфе, распространение идёт и внутри полости живота — трансцеломически.
Не совсем ясно почему злокачественные клетки задерживаются в брюшине, предполагается благотворное действие микроклимата.
Большинство метастазов находят в местах с более спокойной обстановкой и слабой перистальтикой органов, или там, где активно всасывается внутрибрюшная жидкость.
Часто клетки «разбрасываются» во время операции, причём при лапароскопическом вмешательстве вероятность обсеменения вдвое ниже, чем при классической хирургии.
Во время операции обязательно проводится профилактика раковой диссеминации путём неоднократной обработки специальными растворами, но самый эффективный способ очищения от диссеминатов — внутриполостная химиотерапия на фоне гипертермии (HIPEC).
При каких заболеваниях развивается
Перитонеальный канцероматоз диагностируют у каждого третьего пациента с новообразованием желудочно-кишечного тракта. Метастазы по брюшине характерны для карцином желудка и поджелудочной железы — поражается до 40% пациентов.
При раке кишечника канцероматоз обнаруживают только у десятой части больных.
Максимально высокий процент обусловлен злокачественными процессами яичников — на момент выявления болезни две из трёх пациенток уже имеют опухолевые узлы на брюшине.
Вероятность канцероматоза зависит от степени агрессивности раковых клеток и величины первичной опухоли, так при тотальном инфильтративном раке желудка его выявляют чаще, чем при локальном процессе, не разрушившем наружную серозную оболочку органа.
Тем не менее, ни при одном из злокачественных процессов любой локализации, будь то рак молочной железы или простаты, лёгкого или носоглотки, не исключается внутрибрюшинное метастазирование. Посмертно канцероматозные изменения выявляют у каждого третьего, погибшего от прогрессирования заболевания.
Для сарком такая локализация метастазов нетипична, саркоматоз брюшины констатируется едва ли у трёх из сотни больных. В редчайших случаях совершенно доброкачественные по гистологии муцинозные аденома аппендикса и цистаденома яичников тоже способны привести к обсеменению брюшины с выработкой гелеобразного секрета.
У одного из миллиона, и много чаще это будет женщина, выявляют муцинозную аденому аппендикса или муцинозную цистаденому яичников, в последующем часто приводящие к обсеменению брюшины. Распространение аденомуцинозных клеток в полости живота с выработкой гелеобразного секрета именуют уже «псевдомиксома», зачастую при в этой стадии заболевания не удаётся определить первоисточник опухоли.
Диагностика канцероматоза брюшины
Не представляет трудности выявление опухолевого поражения брюшины при асците, в отсутствии выработки патологического секрета диагностика опирается на визуализацию — УЗИ и КТ с контрастированием.
При УЗИ на внутреннем листке, прилежащем к мышцам брюшной стенки, в норме очень тонком и незаметном, можно увидеть напластования толщиной в несколько сантиметров, практически не прослеживаются только мелкие узелки.
КТ с контрастным усилением много информативнее УЗИ, способно выявить сантиметровые образования. Наиболее точный диагностический метод — лапароскопия. Это обследование обязательно при карциноме желудка, при раке яичников предпочтительна операция — диагностика и лечение одновременно.
Для точного определения первоисточника злокачественного процесса исследуется асцитическая жидкость, получаемая при лапароскопии или пункции. Из экссудата выделяют осадок, который изучают под микроскопом и проводят специфические реакции — ПЦР и ИГХ.
На этапе первичной диагностики ПЭТ не всегда информативна, поскольку далеко не все злокачественные клетки легкого, печени, почек способны накапливать изотопы.
Вне всяких сомнений, самый оптимальный метод диагностики — получение кусочка опухолевой ткани для исследования. Биопсия не целесообразна при известном источнике метастазов и после недавнего лечения первичного рака.
Стадии канцероматоза брюшной полости
Стадирование перитонеального канцероматоза нельзя назвать точным, все классификации приблизительны в определении объёма повреждений и не уточняют локализацию узлов.
Зачастую, стадирование даёт общее представление о прогнозе эффективности лечебных мероприятий, нежели информирует о настоящем состоянии внутри полости живота.
Разработанная японскими специалистами градация опухолевого распространения по трём степеням, учитывает общий объём поражения, без числа и размеров очагов:
- P1 — ограниченное;
- P2 — разделённые нормальной тканью очаги;
- P3 — множество узлов.
Во время операции хирурги определяют индекс перитонеального канцероматоза (РСI), измеряя узелки в 13 регионах полости, общая сумма баллов влияет на тактику лечения, в первую очередь, на возможность удаления брюшины — перитонэктомию и целесообразность внутриполостной химиотерапии. При некоторых злокачественных процессах прибегают к сложным формулам расчёта РСI.
Наибольшее представление о размерах ракового повреждения даёт стадирование по степеням:
- 0 — в полости чисто;
- I — в одной анатомической зоне узелки до 5 мм;
- II — множественные узелки до 5 мм;
- III — локальное поражение 0.5–2 см;
- IV — 2-сантиметровые узелки
Течение канцероматоза определяется не столько размером метастатического узла, сколь клеточной потенцией к прогрессии и выработке асцитической жидкости, общей площадью опухолевой трансформации и клиническими проявлениями.
Симптомы канцероматоза брюшной полости
Перитонеальный канцероматоз небольшой протяжённости может не проявлять себя симптомами, особенно в отсутствии выработки асцитической жидкости. С другой стороны, жидкость может продуцироваться и при отсутствии видимых метастазов.
Как правило, симптоматика неспецифична и в разном наборе могут отмечаться:
- меняющие локализацию болезненные ощущения, а чаще — непонятный дискомфорт в полости живота;
- нарастающая слабость до утраты работоспособности;
- потеря веса при стабильном диетическом режиме;
- прогрессирующее снижение аппетита;
- функциональные нарушения со стороны органов ЖКТ.
Дальнейшее нарастание раковых повреждений сопровождается опухолевой интоксикацией, сдавление желудка опухолевыми узлами осложняется тошнотой и рвотой, кишечника — запорами и поносами с усугублением частичной непроходимости. Распад крупных узлов может вызывать боли и повышение температуры.
Асцит нарушает процесс дыхания и вызывает сердечную недостаточность с постоянными отёками, а частая эвакуация патологической жидкости приводит к белковой недостаточности.
Как лечат канцероматоз брюшины
Ни один из современных методов лечения канцероматоза не гарантирует радикального удаления опухоли, не способен излечить, но может улучшить состояние и существенно продлить жизнь.
Хирургическое лечение канцероматоза технически сложное для оперирующей бригады и трудно переносимое пациентом, поскольку предполагает удаление первичного рака, увеличенных лимфатических узлов, сальниковых сумок и всех видимых опухолевых образований вместе с брюшиной.
Перитонэктомия — многоэтапное вмешательство, включающее удаление нескольких органов и отделов брюшной полости. В результате операции пациент может остаться без селезёнки, желчного пузыря, части кишечника, матки с придатками.
Стандарт терапии канцероматоза — химиотерапия системная и локальная — внутрибрюшинная после удаления асцита или через лапаропорт, установленный во время операции. Эффективность лекарственной терапии невысокая, за исключением случаев первичного рака яичников. Таргетные и иммуно-онкологические препараты только изучаются в клинических испытаниях.
Какие методики терапии дают лучший результат
Наиболее высокий эффект демонстрирует комбинация 3 методов лечения рака:
- операция с максимально возможным удалением злокачественных новообразований — циторедукция;
- локальная внутрибрюшинная гипертермия;
- внутриполостное введение химиопрепаратов.
Использование во время хирургического вмешательства интраперитонеальной гипертермической химиотерапии (ИГХТ или HIPEC) позволяет максимально долго поддерживать очень высокую концентрацию цитостатика непосредственно в зоне поражения и усилить лекарственное воздействие нагреванием тканей. При весьма скромных исторических результатах хирургического вмешательства устойчивой к цитостатикам псевдомиксомы только HIPEC открывает пациентам перспективу на долгую жизнь.
Технология ИГХТ такова: в течение полутора часов внутрь брюшной полости под давлением подаётся нагретый химиопрепарат в дозе, существенно превышающей максимально разрешённую для внутривенного введения.
За счёт локального использования изменяется спектр токсических реакций, исключается опасное для жизни повреждение кроветворения, но возможна боль в животе и временное нарушение функционирования органов ЖКТ.
Интраоперационная фотодинамическая терапия (ФДТ), когда на выявленные с помощью фотосенсибилизатора очаги опухоли воздействуют лазером, уступает HIPEC по результативности, поскольку лазером невозможно проникнуть во все «закоулки» брюшной полости. Тем не менее, целесообразно использование фотодинамический терапии при крупных и немногочисленных раковых узлах.
Прогноз при канцероматозном поражении
На течение процесса влияет объём поражения на момент начала терапии, степень злокачественности опухоли, в свою очередь определяющая чувствительность к химиотерапии. Основополагающее влияние оказывает талант и опыт хирурга, и несомненно, правильность выбора лечебной тактики.
Однозначно революционные результаты в клинических испытаниях показала только HIPEC.
После интраоперационной гипертермической ХТ пятилетняя выживаемость при канцероматозе рака желудка выросла максимально до 20%, все прочие методы исключали столь долгое дожитие.
При раке толстой кишки с метастазами по брюшине каждый третий пациент прожил более 5 лет, при карциноме слепой кишки и аппендикса — шестеро из десяти вступили во вторую пятилетку жизни.
Запись
на консультацию
круглосуточно
Список литературы
- Давыдов М.И., Тер-Ованесов М.Д., Буйденок Ю.В. с соавторами/ Гипертермическая интраоперационная интраперитонеальная химиотерапия при раке желудка: существует ли реальная возможность изменить прогноз? // Вестник РОНЦ им. Н. Н. Блохина РАМН; 2010 Т. 21; № 1
- Степанов И.В., Падеров Ю.М., Афанасьев С.Г./ Перитонеальный канцероматоз// Сибирский онкологический журнал; 2014; № 5
- Akiyama H., Yamaoka H., Tanaka K., et al./ Continuous hyperthermic peritoneal perfusion for peritoneal dissemination of gastric cancer // Hepatogastroenterology; 1998.
- Bozzetti F., Bonfanti G., Morabito A., et al/ A multifactorial approach for the prognosis of patients with carcinoma of the stomach after curative resection // Surg. Gynecol. Obstet.; 1986.
- Cotte E., Passot G., Gilly F.N., Glehen O. /Selection of patients and staging of peritoneal surface malignancies // World J. Gastrointest. Oncol.; 2010; Vol. 2.
- Chua T.C., Moran B.J., Sugarbaker P.H., et al. /Early- and longterm outcome data of patients with pseudomyxoma peritonei from appendiceal origin treated by a strategy of cytoreductive surgery and hyperthermic intraperitoneal chemotherapy// J. Clin Oncol 2012.
- Deraco M., Santoro N., Carraro O., Inglese M.G., et al./ Peritoneal carcinomatosis: feature of dissemination. A review // Tumori; 1999.
- Lansom J., Alzahrani N., Liauw W., Morris D.L. /Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy for Pseudomyxoma Peritonei and Appendix Tumours // Indian J Surg Oncol. 2016 Jun.
- Sugarbaker P.H./ Overview of peritoneal carcinomatosis // Cancerologia; 2008.
Источник: https://www.euroonco.ru/terms-from-a-z/kantseromatoz-bryushiny